新东方网>长春新东方学校>优能中学>优能初中>中考资讯>正文
初中化学物质构成的奥秘小结
2016-06-16 09:00
来源:新东方
作者:新东方
初中化学物质构成的奥秘小结由长春新东方同步新东方整理发布,更多精彩内容,请持续关注长春新东方官方网站及长春新东方学校公众号【ccxdfcn】。
本 章 小 节
[归纳整理]
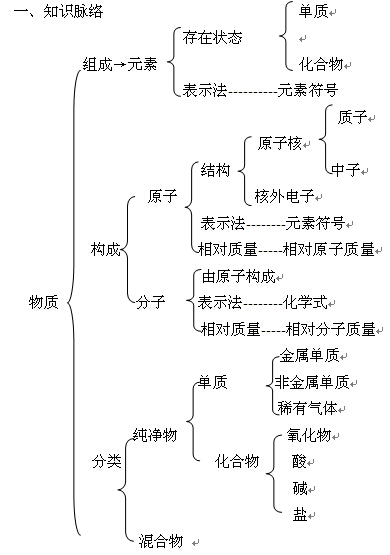
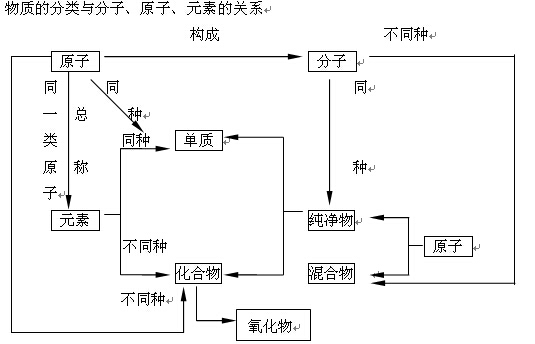
元素分类、性质跟原子结构的关系。
|
原子结构示意图 |
电子层数 |
氢(H) +1 1
|
|
氦(He) +2 2 |
|||||
|
1 |
|||||||||
|
2 |
锂(Li) +3 3
|
铍(Be) +4 2 2 |
硼(B) +5 2 3 |
碳(C) +6 2 4 |
氮(N) +7 2 5 |
氧(O) +8 2 6 |
氟(F) +9 2 7 |
氖(Ne) +10 2 8 |
|
|
3 |
钠(Na) +11281
|
镁(Mg) +12 2 8 2 |
铝(Al) +13 2 8 3 |
硅(Si) +14 2 8 4 |
磷(P) +15 2 8 5 |
硫(S) +16 2 8 6 |
氯(Cl) +17 2 8 7 |
氩(Ar) +18 2 8 8 |
|
|
最外层电子数 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
|
元素分类
|
---金属元素-------------------- ----------非金属元素----------- |
稀有气体元素 |
|||||||
|
结构特征
|
--最外层电子数一般小于4-- --最外层电子数一般多于或是等于4 |
8电子稳定结构(He除外) |
|||||||
|
元素性质 |
-------------易失电子---------- ---------------易得电子------------
|
稳定 |
|||||||
|
形成的微粒 |
阳离子 阴离子 |
/ |
|||||||
|
小结 |
金、少、失 非、多、得 |
稳定 |
|||||||
[问题讨论]
例1.用分子的观点解释酒精挥发和酒精燃烧本质区别。
分析:物理变化和化学变化的根本区别在于变化前后是否生成了其它物质。用分子的观点来区别,就是看变化前后构成物质的分子本身是否起了变化。
答:酒精挥发,只是由于酒精分子运动使分子间的间隙增大了,酒精由液态变成气态,而酒精分子本身并没有改变,所以是物理变化。而酒精燃烧,在燃烧过程中,酒精分子被破坏,分子中的原子和氧分子中的原子重新排列组成了其它物质,生成了二氧化碳分子和水分子,其结果是酒精分子发生了变化,所以酒精燃烧是化学变化。
例2.指出下列符号各表示什么意义:(1)H (2)2H (3)H2O (4)2H2O
分析:按照元素符号和化学式表示的意义以及系数的含义来回答。
答:(1)H:表示氢元素;表示1个氢原子
(2)2H:表示2个氢原子
(3) H2O:表示水;表示水由氢元素、氧元素组成;表示1个水分子;表示1个水分子是由2个氢原子和1个氧原子构成
(4)2H2O:表示2个水分子
例3.将分子、原子、离子、质子、中子、电子等微粒名称填入下列适当空格中:
(1)构成物质的基本微粒是_________________________。
(2)构成原子的基本微粒是_________________________。
(3)显示电中性的微粒有_________________________。
(4)质量最小的微粒是_________________________。
(5)参加化学反应一定发生变化的微粒是_________________________。
(6)原子中数目一定相等的微粒是_________________________。
分析:利用上述微粒的结构、性质等来回答。
答案:(1)分子、原子、离子; (2)质子、中子、电子; (3)中子、分子、原子;
(4)电子; (5)分子; (6)质子和电子。
例4.现有二氧化碳、硫粉、空气、氧气、氧化汞、氯酸钾、海水、铁等8种物质,其中(属纯净物的均写化学式):
(1)属于混合物的是_____________ (2)属于单质的是_____________
(3)属于化合物的是_____________ (4)属于氧化物的是_____________
(5)含有氧分子的物质是_______________________________
(6)由原子构成的单质是_______________________________
分析:利用物质的分类知识及化学式的书写规则完成。
答案:(1)空气、海水;(2)S、O2、Fe;(3)CO2、HgO、KClO3;(4)CO2、HgO;
(5)空气、O2、海水;(6)S、Fe
例5.黑火药是中国古代的伟大发明,它是由木炭、硫粉、硝酸钾配成,回答下列问题:
(1)黑火药是纯净物还是混合物?
(2)黑火药中哪些是单质?哪些是化合物?
(3)黑火药中共含哪几种元素?硝酸钾中各元素的质量比及氧元素的质量分数各是多少解:(1)属于混合物;(2)单质为木炭、硫,化合物为硝酸钾;
(3)黑火药中共含有碳、硫、钾、氮、氧五种元素。
KNO3中钾氮氧三种元素的质量比=39:14:16×3
=39:14:48
KNO3中氧元素的质量分数=
=![]()
=![]()
=47.5%
[单元练习]
可能用到的相对原子质量:Se:79 C:12 N:14 O:16 H:1 I:127 K:39
一、选择题(每小题只有1个选项符合题意)
1.氧化汞受热时的变化可用图表示(图中大圆圈表示汞原子,小圆圈表示氧原子)。据图得出的下列结论错误的是 ( )
A.氧化汞受热时能分解成汞和氧气 B.原子是化学变化中的最小微粒
C.分子在化学变化中可以再分 D.所有的物质都是由分子构成
2.下列现象中不能用分子运动论解释的是( )
A.把两块表面平滑干净的铅压紧,就不容易将它们拉开
B.在室内,同样表面积的热水比冷水蒸发得快
C.氧化汞受热分解生成汞和氧气
D.医院里充满了酒精味和药味
3.干燥多风季节夜晚,在荒野里,人们有时可看到“鬼火”现象,其实它是一种类似与氨气组成的气体(PH3)在空气中的自燃现象,则PH3中P的化合价是 ( )
A.+3价 B.-3价 C.+1价 D.+5价
4.曾用作麻醉剂的“笑气”是一种氮氧化物,其中氮元素的化合价为+1价,“笑气”的化学式是 ( )
A.N2O5 B.NO2 C.NO D.N2O
5.下列说法中,若以质量分数比较,错误的是 ( )
A.空气中含量最多的元素是氮 B.地核里含量最多的元素是氧
C.矿泉水中含量最多的元素是钙 D.海水中含量最多的元素是氧
二、填空题
6.按要求用正确的化学符号表示:
(1)2个氮原子_________; (2)铵根离子___________;
(3)地核中含量最多的金属元素_______; (4)1个硫酸分子____________;
(5)硝酸汞中正二价的汞元素________; (6)3个亚铁离子____________;
(7)构成氯化钠晶体的阴离子_______; (8)由硫离子与亚铁离子构成的物质______。
7.焚烧生活垃圾会产生二恶英,其中毒性较大的一种物质化学式是C12H4O2Cl4,该物质中氢、碳元素的原子个数比为____________,氯、氧元素的质量比为__________。
8.硒元素具有抗衰老、抑制癌细胞生长的功能,已知硒的元素符号为Se,其含氧酸的化学式为H2SeO4,则硒元素的化合价为________,该酸一个分子中所含原子的总数为____个,组成该酸的H、Se、O元素质量比为_____________。
9.已知毒品海洛因的化学式为C21H23NO5,它由____种元素组成,相对分子质量为____,其中氮的质量分数为______,它应属于______物。
10.如图所示的装置久放之后,烧杯甲中的溶液变
______色,烧杯局中溶液的溶质的质量分数将______
(填大或小)
三、简答题
11.邪教头目李洪志宣称,练他的法轮功后能将铜分子、铝分子变成黄金。请你根据科学知识反驳其荒唐性。
12.古罗马人的平均寿命很短,只有廿余年。你认为这可能主要跟以下哪些因素有关?为什么?
(1)古罗马上空的空气污染严重。
(2)古罗马人营养很差。
(3)古罗马城市中用铅作水管,用铅制器皿饮水。
13.下表列出了四种金属元素的原子结构及单质的性质等具体情况:
|
元素名称 |
元素符号 |
原子结构示意图 |
密度(g/mL) |
熔点(℃) |
沸点(℃) |
冷水反应 |
|
锂
|
Li |
+3 2 1 |
0.534 |
180.5 |
1347 |
剧烈 |
|
钠
|
Na |
+11 2 8 1 |
0.97 |
97.81 |
832.9 |
剧烈 |
|
钾
|
K |
+19 2 8 8 1 |
0.86 |
63.65 |
774 |
剧烈 轻微爆炸 |
|
铷
|
Rb |
+37 2 8 18 8 1 |
1.532 |
38.89 |
688 |
剧烈 发生爆炸 |
按以上表列资料分析,你发现了哪些规律性:
(1)______________________________________________________________________
(2) ______________________________________________________________________
(3) ______________________________________________________________________
四、计算题
14.在食盐中加入适量的碘酸钾(KIO3),可以有效地防治碘缺乏病。KIO3的相对分子质量为______,KIO3中各元素的质量比为________,其中碘元素的质量分数为________(保留三位有效数字),我国规定每Kg食盐中含碘0.035g,相当于每Kg食盐含碘酸钾______g。
15.近年来,乳酸成为人们研究的热点之一,乳酸在医药、食品等工业中应用前景广阔,乳酸的化学式为C3H6O3,试计算:
(1)乳酸中碳、氢、氧元素的质量比
(2)乳酸中碳元素的质量分数
16.(1)通过计算比较硝酸铵(NH4NO3)与尿素[(NH2)2CO]哪个含氮量高?(2)为满足生产需要,要使每公顷地增加2kg的氮元素,问在50hm2地上适宜施何种氮肥?施多少kg?
参考答案提示
第一节 练习测试
1.C 2.C
3.这3类5种洗涤用品混合后发生了化学反应,生成氯气,而氯气由于运动于空气被人吸入而中毒。在使用洗涤用品时,不能随意混合使用。
4.主要从物质的微粒之间有间隔考虑。
5.答案很多,只要符合题意均可。
6.(1)打开香水瓶盖,由于香水中微粒不断运动,分散到空气里被人呼入。
(2)由于碳墨水的微粒不断运动,分散到水分子的间隔里,故逐渐溶解而变黑。
(3)味精中微粒由于不断运动而扩散到菜汤微粒的间隙里,故可感觉到味精的鲜味。
(4)因为太阳晒着的地方温度高,微粒运动的动能增大,故水中的微粒易运动而扩散到空气中。
(5)防止因酒精、汽油里的微粒由于不断运动而散失。
(6)瓶里还应存在空气,瓶壁附有水。
第二节 练习测试
1.C 2.D 3.D 4.61
5.分子 分子 原子 原子 原子 原子 分子。 原子 原子核 电子。
质子 中子 电子 原子。
6.(1)在原子里质子数等于核外电子数
(2)不同种原子的质子数不同
(3)相对原子质量通常等于质子数与中子数之和。
(4)不同种类原子数相对质量一般不相同。等等
7.答:水通电是由于水分子在直流电的作用下分解氢原子和氧原子,而每两个氢原子和两个氧分子分别构成了1个氢分子和1个氧分子,许许多多的分子聚集成氢气和氧气,分子变了发生了化学变化。而水蒸发是由于水分子不断运动而散发到空气里,水由液态变成了气态。水分子本身改变属物理变化。
8.由于二氧化碳分子不断运动,分散到水分子间的间隙里,使得气体体积减小,气压减小,故瓶子瘪了。
9.[提示]科学是反映自然、社会、思维等客观规律的分科的知识体系。
恩格斯所以认为“化学的新世纪开始于原子学说”。是因为在18世纪的后半期,化学研究中普遍应用了天平之后,开始重视定量研究,从而对物质的变化和性质有了较深入、较细致的认识。19世纪的前50年代左右,化学从定性研究的方法或观点逐步向定量研究的方法和观点发展,以弄清物质的组成及化学变化中反应物之间和反应物、生成物之间量的关系为目的,由此建立了像质量守恒定律、定比定律、信比定律、化含量定律等一些基本化学定律。为了进一步揭示这些基本定律之间的内在联系和本质,道尔顿提出了近代原子学说。这一学说经过尔后的不断完善,终于成为当时说明各种化学现象的统一理论。所以说,它标志着近代化学发展的新起点。
10.油气炸弹爆炸时释放了大量可燃性气体,而大量可燃性气体引爆时消耗了大量氧气,使防空工事里缺氧,造成人的窒息死亡。
第三节 练习测试
1.B 2.B 3.B 4.C
5.核外电子,16,3,6;质子数,最外层的电子数
6.碳和氢两种,氧。
7.
|
|
定义 |
关系 |
举例 |
|
含氧化合物 |
含有氧元素的化合物 |
共同点:都含有氧元素的化合物 |
KClO3为含氧化合物,但不属氧化物 |
|
氧化物 |
由两种元素组成,其中有一种是氧元素的化合物 |
不同点:含氧化合物不一定是氧化物 |
SO2既是含氧化合物,又是氧化物 |
8.(1)⑥⑦⑨ (2)①②③④⑤⑧⑩ (3)③⑤⑧ (4)③⑧ (5)⑩ (6)①②④
9.(1)不正确。如Mg2+、Cl-等离子最外层电子数也为8个。
(2)正确
(3)不正确。2H表示2个氢原子,2H+表示2个氢离子,H2表示氢气或氢分子,所以化学性质不同。
10.(1)A为镁原子Mg B为氖原子Ne C为氟原子F
(2)氖原子性质稳定,因最外层8个电子,镁原子易失电子,因为最外层只有2个电子,氟原子因为最外层有7个电子与8电子结构只差1个,所以易得电子。
11.(1)炼铜原料中一定含有铅、铜、锌等元素。
(2)不能,因为外地受污染的蔬菜也会进入本地。
(3)应按照谁污染谁治理的原则进行治理整顿,做到达标排放,否则要实行关、停、并、转。
第四节 练习测试
1.A 2.B 3.D
4.H2; H、O; H2O; H+、OH-; H+
5.四 11 61
6.从上到下填入代号:D、B、C、A、E
7.略。
8.重点抓住NaCl中氯原子得到1个电子成为带1个负电荷的氯离子(Cl-)而显-1价,而HCl是氢、氯原子各出1个电子形成的共用电子,偏向氯而使氯原子显负电性,Cl显-1价。
9.过氧化氢与水均属由氢氧两种元素组成的氧化物,但由于分子构成不同、物质不同,故化学性质不同。
10.CO、CO2;CO、O2;CO、CO2、O2;CO、O3;CO、CO2、O3;CO、O2、O3;
CO、CO2、O2、O3、
11.(1)Fe2O3中铁氧朱子个数比为2:3 元素质量比为7:3(112:48)
(2)Fe%=70% O%=30%
(3)56g (4)40g (5)200t
12.实际含氮量为96.4%>96% 可按一级品出售。
单元练习
一、选择题
1.D 2.A 3.B 4.D 5.C
二、填空题 +2
6.(1)2N (2)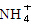 (3)Al (4)H2SO4 (5)Hg(NO3)2 (6)3Fe2+
(3)Al (4)H2SO4 (5)Hg(NO3)2 (6)3Fe2+
7. 1:3 142:32(或71:16)
8. +6 7 2:79:64
9. 四 369 3.8% 化合物或含氧化合物或有机物
10. 红 变小
三、简答题
11.答:(1)铜、铝均由原子构成,不能讲由分子构成。
(2)化学变化的实质是原子重新组合,元素种不变,所以铜、铝不可能变成金。
12.主要与(3)有关,因为人体内吸入过量的铅引起的中毒。
13.(1)Li、Na、K、Rb原子最外层电子数相同
(2)随核电荷数增加,核外电子层数依次增加。
(3)熔、沸点依次减小,与冷水反应的剧烈程度依次增强。
四、计算题
14. 214 39:127:48 59.3% 0.06
15. (1)6:1:8 (2)40%
16. (1)NH4NO3:N%=35% (NH2)CO中N%=46.7%
尿毒的含氮量高
(2)宜施尿素,约214.3kg。
相关推荐
以上就是本文的全部内容,更多精彩内容,请持续关注长春新东方网。

新东方长春学校官方微信:新东方长春学校 (微信号:ccxdfcn)
最新考试资讯、考试政策解读、真题解析,请扫一扫二维码,关注我们的官方微信!
相关推荐
版权及免责声明
①凡本网注明"稿件来源:新东方"的所有文字、图片和音视频稿件,版权均属新东方教育科技集团(含本网和新东方网) 所有,任何媒体、网站或个人未经本网协议授权不得转载、链接、转贴或以其他任何方式复制、发表。已经本网协议授权的媒体、网站,在下载使用时必须注明"稿件来源:新东方",违者本网将依法追究法律责任。
② 本网未注明"稿件来源:新东方"的文/图等稿件均为转载稿,本网转载仅基于传递更多信息之目的,并不意味着赞同转载稿的观点或证实其内容的真实性。如其他媒体、网站或个人从本网下载使用,必须保留本网注明的"稿件来源",并自负版权等法律责任。如擅自篡改为"稿件来源:新东方",本网将依法追究法律责任。
③ 如本网转载稿涉及版权等问题,请作者见稿后在两周内速来电与新东方网联系,电话:010-60908555。